Maklum Balas FDA Menyokong Penyerahan Kebenaran Penggunaan Kecemasan (EUA) Terancang ADG20 untuk Pencegahan COVID-19; Pakej Data Klinikal Interim daripada Ujian Pencegahan EVADE akan Menyokong Penyerahan EUA yang Dijangkakan pada Suku Kedua 2022Pendaftaran Ujian STAMP ADG20 untuk Rawatan COVID-19 Sedang Berjalan Dengan Baik; Analisis Keberkesanan Interim Terancang Dijangka Dikeluarkan pada Suku Kedua 2022 untuk Menyokong Potensi Penyerahan EUAWALTHAM, Massachusetts, 17 Nov (Bernama-GLOBE NEWSWIRE) -- Adagio Therapeutics, Inc., (Nasdaq: ADGI) sebuah syarikat biofarmaseutikal peringkat klinikal yang tertumpu pada penemuan, pembangunan dan pengkomersialan penyelesaian berasaskan antibodi untuk penyakit berjangkit dengan potensi pandemik, hari ini mengumumkan perkembangan terkini tentang program antibodi COVID-19 utamanya iaitu ADG20 dan melaporkan keputusan kewangan suku ketiga tahun 2021. ADG20 ialah calon produk antibodi monoklon percubaan yang direka cipta untuk menghasilkan aktiviti peneutralan yang meluas dan kuat terhadap SARS-CoV-2, termasuk varian membimbangkan untuk pencegahan dan rawatan COVID-19.
“ADG20 terus menjadi satu-satunya antibodi monoklon dalam peringkat akhir pembangunan yang berpotensi untuk menawarkan gabungan potensi yang unik, keluasan peneutralan pada pelbagai varian membimbangkan SARS-CoV-2 serta virus seumpama SARS tambahan dengan potensi pandemik, serta perlindungan berkekalan terhadap COVID-19 hingga satu tahun. Selain itu, penyampaian suntikan tunggal kami mengelakkan kesulitan yang berkaitan dengan pentadbiran IV atau suntikan berbilang,” kata Lynn Connolly, M.D., Ph.D., Ketua Pegawai Perubatan Adagio. “Dunia terus menghadapi pelbagai cabaran dalam menangani krisis COVID-19 sepenuhnya. Alternatif atau tambahan kepada vaksin untuk mencegah COVID-19 diperlukan untuk individu dengan sistem imun yang lemah dan mereka yang masih teragak-agak untuk menerima vaksin atau membenarkan vaksin terhadap anak-anak mereka. Populasi pesakit tertentu mungkin bukan merupakan calon yang sesuai untuk pilihan rawatan secara oral yang semakin banyak memuncul kerana masalah pematuhan, komorbiditi atau interaksi ubat yang mungkin terjadi. Berdasarkan gabungan ciri-cirinya, ADG20 berpotensi sebagai alternatif yang berbeza untuk mencegah dan merawat COVID-19 yang mampu memenuhi keperluan populasi ini dan komitmen kami terhadap perkembangannya tidak pernah pudar.”
“Kami telah mencapai kemajuan yang signifikan sepanjang tahun 2021 dan 2022 akan menjadi tahun yang penting bagi Adagio ketika kami bersiap sedia untuk menyerahkan potensi EUA ADG20 sebagai kaedah pencegahan dan rawatan COVID-19,” kata Tillman Gerngross, Ph. D., pengasas bersama dan Ketua Pegawai Eksekutif Adagio. “Baru-baru ini, kami menerima maklum balas yang jelas daripada FDA tentang strategi menyerahkan EUA ADG20 sebagai alat pencegahan COVID-19, dan telah memulakan usaha untuk mengembangkan program klinikal kami kepada subset pesakit tambahan termasuk individu dan kanak-kanak yang terimunokompromi atau mengalami kelemahan imun. Usaha ke arah kesediaan komersial kami sedang berjalan dengan baik dan dengan kunci kira-kira yang mantap, kami bersedia untuk bergerak dengan pantas bagi mendayakan akses terhadap individu yang memerlukan pilihan pencegahan dan rawatan COVID-19, jika kebenaran dan/atau kelulusan diberikan.”
Kemas Kini Program COVID-19 ADG20PencegahanAdagio terus mendaftarkan peserta dewasa dan remaja dalam ujian klinikal EVADE Fasa 3 globalnya yang sedang berlangsung yang menilai ADG20 sebagai kaedah pencegahan COVID-19 dalam kedua-dua keadaan prapendedahan dan pendedahan terkini.
· Adagio telah menerima maklum balas daripada Pentadbiran Makanan dan Ubat-ubatan (FDA) A.S. tentang pakej data yang diperlukan serta proses penyerahan EUA untuk pencegahan prapendedahan COVID-19
· Adagio menjangkakan bahawa pakej data untuk menyokong EUA ADG20 akan tersedia pada suku kedua 2022 diikuti dengan penyerahan kepada FDA yang dijangkakan pada suku ketiga 2022
· Adagio merancang untuk menambah kohort baharu dalam EVADE bagi menilai ADG20 sebagai suatu pilihan pencegahan bagi individu yang mengalami kelemahan imun dengan pendaftaran yang dijangka akan bermula pada suku pertama tahun 2022
· Adagio juga merancang untuk memulakan ujian yang menilai ADG20 sebagai vaksin tambahan
· Susulan perbincangan dengan pihak FDA, Adagio telah menyelaraskan suatu perancangan untuk menilai ADG20 sebagai pilihan pencegahan pada populasi kanak-kanak, dengan percubaan ke atas individu berumur antara dua hingga 11 tahun yang dijangka akan dimulakan pada pertengahan tahun 2022
RawatanAdagio terus mendaftarkan pesakit dalam ujian klinikal STAMP Fasa 2/3 globalnya yang sedang berjalan, bagi menilai ADG20 sebagai rawatan untuk COVID-19.
· Adagio merancang untuk mengubah suai reka bentuk ujian ini bagi memperluas populasi pesakit berisiko yang layak untuk didaftarkan dalam STAMP
· Berdasarkan pendaftaran semasa, Adagio menjangkakan untuk memperoleh penilaian jawatankuasa pemantauan data bebas Fasa 2 pada suku pertama 2022 manakala analisis keberkesanan interim pula pada suku kedua 2022 untuk menyokong penyerahan EUA berikutnya
Pembentangan Data ADG20 Terkini di ISIRV-WHO dan IDWeek2021· Data
in vitro baharu menunjukkan aktiviti peneutralan dikekalkan oleh ADG20 terhadap suatu panel dengan pelbagai varian SARS-CoV-2 yang beredar, termasuk varian Lambda, Mu dan Delta plus yang baru muncul. Hasilnya, penemuan menunjukkan bahawa ADG20 menunjukkan aktiviti peneutralan yang kuat terhadap semua varian membimbangkan SARS-CoV-2 yang diuji, termasuk individu yang mempunyai kerentanan berkurangan terhadap produk mAb yang kini tersedia di bawah EUA atau masih dalam pembangunan peringkat akhir.
· Data daripada
penilaian selama enam bulan dalam ujian Fasa 1 ADG20 Adagio pada sukarelawan yang sihat mengesahkan pelanjutan separuh hayat ADG20, yang menghampiri 100 hari berdasarkan data daripada dos intramuskular sebanyak 300 mg yang diberikan dalam bentuk satu suntikan tunggal. Di samping itu, analisis penerokaan menunjukkan bahawa 50% peneutralan virus serum yang menitrasi pada bulan keenam selepas pengedosan intramuskular 300 mg ADG20 adalah serupa dengan titrasi kemuncak yang diperhatikan pada vaksin mRNA-1273 dan mengatasi pencapaian siri vaksin AZD1222. ADG20 diterima dengan baik tanpa sebarang kesan mudarat yang berkaitan dengan ubat (AE), AE yang serius, atau tindak balas hipersensitif atau tapak suntikan yang dilaporkan melalui sekurang-kurangnya tiga bulan tindakan susulan pada keseluruhan kohort.
· Untuk menyokong
pilihan dos bagi ujian klinikal Fasa 2/3 STAMP dan EVADE Adagio di seluruh dunia, syarikat telah mengubah suai sistem farmakologi kuantitatif sedia ada pada model farmakokinetik (QSP/PBPK) seluruh badan berasaskan fisiologi untuk mencirikan PK bagi mAb separuh hayat yang dilanjutkan dalam serum dan lokasi utama replikasi virus pada saluran pernafasan. Model Adagio menjangkakan
a priori PK serum ADG20 yang secukupnya diperhatikan pada primat bukan manusia (NHP) dan manusia. Model ini seterusnya dioptimumkan berdasarkan data daripada ujian klinikal Fasa 1 Adagio dan kemudian digunakan untuk pemilihan dos STAMP dan EVADE, yang akhirnya memberikan maklumat tentang pemilihan dos intramuskular 300 mg ujian ini.
Harta IntelekPada 29 Oktober 2021, Pejabat Paten dan Tanda Dagangan Amerika Syarikat telah menghantar notis kebenaran kepada syarikat untuk memohon paten yang akan memberikan perlindungan paten kepada ADG20 di A.S.
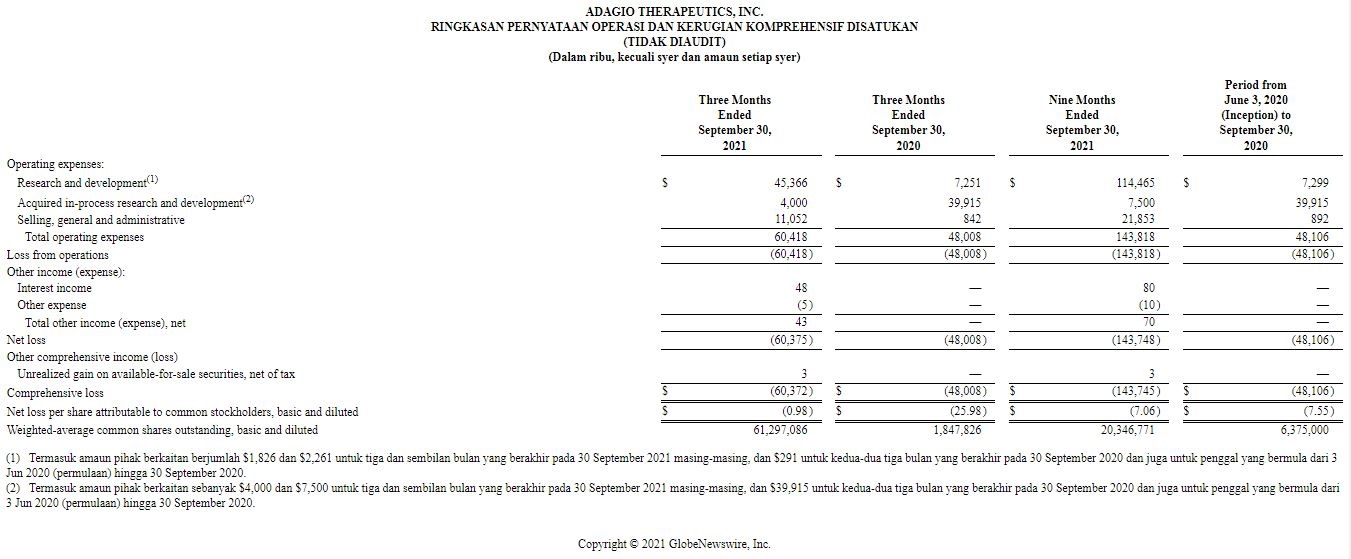
Keputusan Kewangan Suku Tahun Ketiga 2021· Setakat 30 September 2021, Adagio mempunyai tunai, kesetaraan tunai dan sekuriti boleh dipasarkan yang bernilai $666.3 juta dan dijangka akan menyokong rancangan operasi semasa syarikat hingga tahun 2023.
· Perbelanjaan penyelidikan & pembangunan termasuk penyelidikan dan pembangunan yang sedang dalam proses untuk suku ketiga tahun 2021 berjumlah $49.4 juta.
· Perbelanjaan penjualan, perbelanjaan am & pentadbiran untuk suku ketiga tahun 2021 ialah $11.1 juta.
· Kerugian bersih untuk suku ketiga berjumlah $60.4 juta, atau $0.98 setiap syer.
Tentang ADG20ADG20 ialah percubaan antibodi monoklon yang menyasarkan protein pepaku SARS-CoV-2 dan koronavirus yang berkaitan, yang sedang berkembang maju melalui ujian klinikal global bagi pencegahan dan rawatan COVID-19, penyakit yang dibawa oleh SARS-CoV-2. ADG20 direka cipta dan direkayasa untuk memiliki potensi yang tinggi serta melakukan aktiviti peneutralan yang meluas terhadap SARS-CoV-2 dan sarbekovirus klad 1 tambahan dengan menyasarkan epitop yang sangat terpelihara dalam domain yang mengikat reseptor. ADG20 telah direkayasa selanjutnya untuk menghasilkan pelanjutan separuh hayat bagi perlindungan yang bertahan lama. ADG20 telah menunjukkan aktiviti peneutralan yang kuat terhadap virus asal SARS-CoV-2, kesemua varian membimbangkan SARS-CoV-2 yang diketahui dan virus tambahan yang sama seperti SARS dalam kajian praklinikal. ADG20 diberikan melalui suntikan intramuskular tunggal dalam ujian klinikal. Setakat ini, ADG20 telah diterima dengan baik dalam ujian Fasa 1 tanpa apa-apa petunjuk keselamatan yang dikenal pasti melalui tindakan susulan selama sekurang-kurangnya tiga bulan pada seluruh kohort. ADG20 belum diluluskan untuk digunakan di mana-mana negara dan keselamatan serta keberkesanannya masih belum ditentukan.
Tentang Adagio TherapeuticsAdagio (Nasdaq: ADGI) ialah sebuah syarikat biofarmaseutikal peringkat klinikal yang tertumpu pada penyelidikan, pembangunan dan pengkomersialan penyelesaian berasaskan antibodi untuk penyakit berjangkit dengan potensi pandemik termasuk COVID-19 dan influenza. Portfolio antibodi syarikat ini telah dioptimumkan menggunakan keupayaan kejuruteraan antibodi Adimab yang terkemuka dalam industri dan direka cipta untuk menyediakan para pesakit dan doktor dengan gabungan potensi, keluasan, perlindungan yang bertahan lama (melalui pelanjutan separuh hayat) serta kebolehbuatan dan kemampuan yang mengagumkan. Portfolio antibodi SARS-CoV-2 Adagio termasuk antibodi berbilang yang tidak bersaing serta melakukan peneutralan secara meluas dengan epitop pengikat yang berbeza yang didorong oleh ADG20. Adagio telah memperoleh kapasiti pengeluaran untuk menghasilkan ADG20 dengan pengilang pihak ketiga secara kontrak untuk menyokong penyempurnaan ujian klinikal serta pelancaran komersial peringkat awal bagi memastikan potensi akses yang meluas kepada orang ramai di seluruh dunia. Untuk maklumat lanjut, sila layari
www.adagiotx.com.
Pernyataan Berpandangan Ke HadapanSiaran akhbar ini mengandungi pernyataan yang berpandangan ke hadapan dalam lingkungan pengertian Akta Pembaharuan Litigasi Sekuriti Swasta 1995. Perkataan seperti "meramal," "percaya," "menjangkakan," "bertujuan," "projek," dan "masa depan" atau ungkapan yang serupa, bertujuan untuk mengenal pasti pernyataan yang berpandangan ke hadapan. Kenyataan yang berpandangan ke hadapan termasuk pernyataan tentang masa, perkembangan serta hasil kajian praklinikal dan ujian klinikal ADG20 kami, termasuk masa penyerahan EUA yang kami rancang, permulaan, pengubahsuaian dan penyempurnaan kajian atau ujian dan kerja-kerja penyediaan yang berkaitan, jangka masa ketersediaan hasil ujian serta program penyelidikan dan pembangunan kami; keupayaan kami untuk memperoleh dan mengekalkan kelulusan kawal selia untuk calon produk kami; keupayaan kami untuk mengenal pasti pesakit termasuk populasi pesakit tertentu dengan penyakit yang dirawat oleh calon produk kami serta keupayaan untuk mendaftarkan para pesakit ini dalam ujian klinikal kami; jangkaan kami tentang skop sebarang petunjuk yang diluluskan untuk ADG20; dan manfaat calon produk kami kepada pesakit; keupayaan dan strategi pembuatan kami; dan keupayaan kami untuk mengkomersialkan calon produk kami dengan jayanya. Kami mungkin tidak dapat mencapai rancangan, tujuan atau jangkaan sebenar yang didedahkan dalam pernyataan berpandangan ke hadapan kami dan anda tidak boleh meletakkan pergantungan yang tidak wajar terhadap pernyataan berpandangan ke hadapan ini. Pernyataan berpandangan ke hadapan ini melibatkan risiko dan ketidakpastian yang boleh menyebabkan keputusan sebenar kami berbeza secara material daripada keputusan yang diterangkan atau yang tersirat dalam pernyataan berpandangan ke hadapan ini, termasuk dan tidak terhad kepada kesan pandemik COVID-19 ke atas perniagaan, ujian klinikal dan kedudukan kewangan kami serta data keselamatan yang tidak dijangka atau keberkesanan yang diperhatikan semasa kajian praklinikal atau ujian klinikal, pengaktifan tapak ujian klinikal atau kadar pendaftaran yang lebih rendah daripada yang dijangkakan, perubahan pada persaingan yang dijangka atau sedia ada, perubahan pada persekitaran kawal selia dan ketidakpastian serta jangka masa proses kelulusan kawal selia. Faktor lain yang boleh menyebabkan keputusan sebenar kami berbeza secara material daripada yang dinyatakan atau yang tersirat dalam pernyataan berpandangan ke hadapan dalam siaran akhbar ini diterangkan di bawah tajuk "Faktor Risiko" dalam Laporan Suku Tahunan Adagio pada Borang 10-Q untuk suku tahunan yang berakhir pada 30 Jun 2021 dan dalam laporan akan datang Adagio yang akan difailkan dengan SEC, termasuk Laporan Suku Tahunan Adagio pada Borang 10-Q untuk suku tahunan yang berakhir pada 30 September 2021. Risiko sedemikian mungkin meningkat akibat pandemik COVID-19. Pernyataan berpandangan ke hadapan yang terkandung dalam siaran akhbar ini dibuat hanya pada tarikh ini dan Adagio tidak bertanggungjawab untuk mengemas kini maklumat tersebut kecuali jika diperlukan di bawah undang-undang yang berkuatkuasa.Sila hubungi:Hubungan Media:Dan Budwick, 1AB
Dan@1abmedia.comHubungan Pelabur:Monique Allaire, THRUST Strategic Communications
monique@thrustsc.com
 Sumber: Adagio Therapeutics, Inc.--BERNAMA
Sumber: Adagio Therapeutics, Inc.--BERNAMA